
诸多研究正在将与自免相关的炎症靶点和PROTAC两者相结合,比较热门的靶点是HDAC VI、IRAK3/4、PCAF、GCN5、JAK/STAT、RIPK2、STING、MIF、IKZF,针对这些靶点设计开发用于自免治疗的PROTACs,在临床前阶段显示出良好的体外效力。
引言:
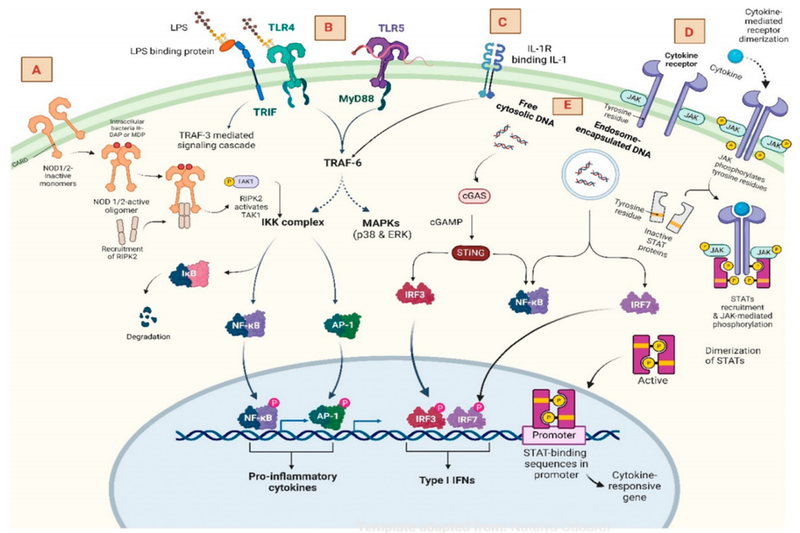
PROTAC(Proteolysis Targeting Chimeras,蛋白降解靶向嵌合体)是一种创新的蛋白质降解技术,其结构由三部分组成:一端是与目标蛋白(POI)结合的配体,另一端是与特定的E3泛素连接酶结合的配体,中间通过一个Linker(连接子)相连。这种设计使得PROTAC分子能够同时结合目标蛋白和E3泛素连接酶,从而促进目标蛋白的泛素化,并通过泛素-蛋白酶体途径(UPS)实现目标蛋白的选择性降解。

通过设计特定的PROTAC分子,可以诱导与自身免疫性疾病相关的靶蛋白降解,从而为治疗这些疾病提供新的策略。在设计和评估PROTAC分子时,研究人员会关注其诱导靶蛋白降解的能力,这通常通过DC50(半最大降解浓度)和Dmax来量化。DC50是指能够导致目标蛋白降解50%的PROTAC浓度,而Dmax则表示在饱和浓度下PROTAC能实现的最大降解水平。现将HDAC VI、IRAK3/4、PCAF、GCN5、JAK/STAT、RIPK2、STING、MIF、IKZF靶点的临床前PROTACs开发情况介绍如下:
1 HDAC VI(组蛋白去乙酰化酶6)
组蛋白去乙酰化酶(HDAC)是一类重要的酶,它们通过去除组蛋白上的乙酰基团来调控基因的表达。HDAC的功能异常与多种疾病的发生发展有关,尤其是癌症。阻断HDAC可导致细胞死亡和抗炎活性。用于癌症治疗的强效HDAC抑制剂,TSA(Trichostatin A)、SAHA(Suberoylanilide Hydroxamic Acid)等,可以减少诱导关节炎大鼠的肿胀、血管形成和骨侵蚀。
HDAC VI是目前与自身免疫性疾病关联最大的HDAC家族成员,负责炎症的调节,阻断HDAC VI可治疗类风湿性关节炎,以改善滑膜炎症。以下是针对HDAC V1靶点的PROTAC开发情况:
Compound2:Cao等人引入了“点击”化学的概念,合成了由不同连接子长度组成的PROTAC分子。其中化合物2的体外研究显示,DC50为108.9 nM,能够显著降解HDAC VI,以及减少 IL-1β(白细胞介素-1β)的释放和p20(caspase-1的中间体片段)的产生;体内研究表明,化合物2降低IL-1β水平,而不影响TNF- α(肿瘤坏死因子-α)水平。
Compound3:Yang等人合成的PROTAC分子,以来那度胺作为配体与CRBN(E3连接酶配体)结合,DC50为1.9 nM,显著降解HDAC VI。
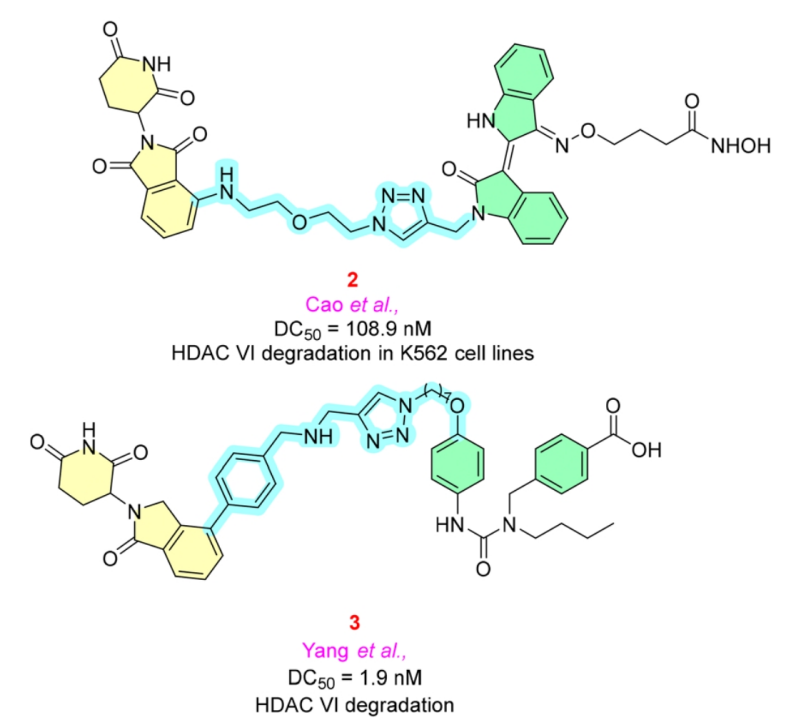 图3 靶向HDAC VI的PROTACs
图3 靶向HDAC VI的PROTACs2 IRAK3/4(IL-1受体相关激酶)
IRAK(Interleukin-1 receptor-associated kinase)是与IL-1R和Toll样受体(TLR)信号传导相关的一类丝氨酸-苏氨酸蛋白激酶。IRAK家族成员通过激活下游的信号转导分子如NF-κB和MAPK途径,在调节炎症反应和免疫反应中起着关键作用。其中IRAK-4尤其重要,因为它是固有免疫系统中IL-1家族和TLR家族信号通路交汇的关键节点,参与全身炎症反应的调控。IRAK4蛋白涉及类风湿关节炎和化脓性汗腺炎(HS),是目前治疗免疫疾病的深入研究课题。由于IRAK1和IRAK4的ATP结合位点之间的高度相似性,IRAK4的选择性抑制剂或可治疗系统性红斑狼疮。
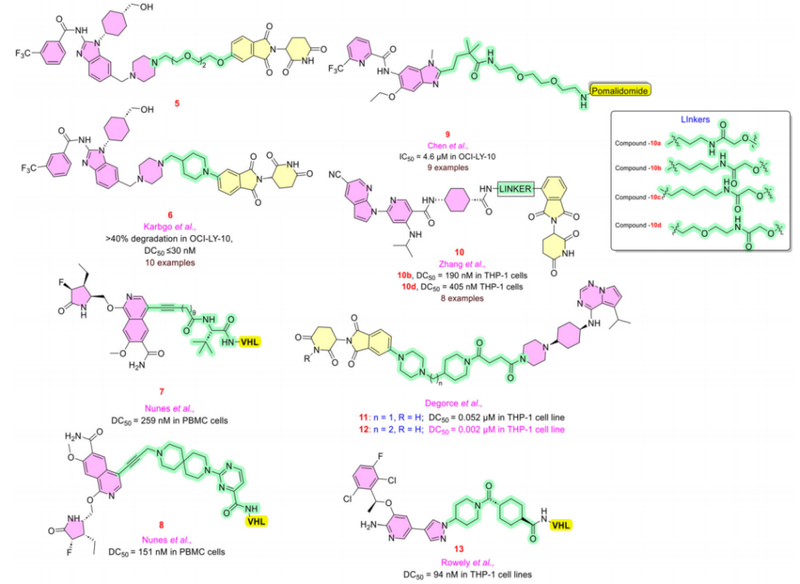
Compound5、6:Kargbo等认为,PROTAC可以克服IRAK4蛋白的催化结构域高度保守的限制,开发的化合物5、6可有效降解IRAK4,IC50和DC50值低于30 nM。
Compound7、8:Nunes等人使用异喹啉弹头(IRAK4抑制剂)和各种E3配体,如VHL(VonHippel-Lindau)、CRBN或IAP(凋亡抑制剂蛋白)。其中,含有氟基团的化合物7的DC50为259 nM。进一步细化结构,化合物8采用螺旋环嘧啶连接子,比柔性的线性碳链更具刚性和极性,DC50为151 nM。
Compound9:Chen等人研究发现,采用更短长度连接子的PROTACs并没有观察到IRAK4的显著降解,而含有PEG(聚乙二醇)连接子的化合物9可以有效地降低IRAK4的水平。
Compound10:Zhang等人,将环丙基作为连接子偶联位点,化合物10抑制了IL-6的产生;接着改变连接子,合成一系列PROTACs,其中化合物10b和10d的DC50值为190 nM和405 nM。
Compound11、12:Degorce等人在研究IRAK4蛋白时,偶然发现IRAK3抑制剂治疗自免疾病的功效。POI配体采用吡咯三嗪的顺式异构体,E3连接酶配体采用VHL或CRBN。研究表明,含有PEG连接子的CRBN比VHL具有更好的降解能力,且在采用CRBN的情况下,连接子的长度与降解效果成正比。化合物11和12选择性降解IRAK3,DC50分别为0.052 μM和0.002 μM,Dmax分别为74%和98%。
Compound13:Rowley等人也做出了类似的努力,他们研究了IRAK3蛋白来控制树突状细胞介导的IL-12。采用克唑替尼作为POI配体,VHL作为E3连接酶配体,反式环己酰胺作为连接子,化合物13能够有效降解IRAK3,DC50为94 nM和 Dmax为95%。用化合物13处理树突状细胞后,无论LPS(脂多糖)存不存在,IRAK3均被降解,同时在LPS刺激下,IL-12p水平显著升高。
3 PCAF和GCN5(p300/cbp相关因子和组蛋白乙酰转移酶)
PCAF和GCN5是密切相关的表观遗传蛋白,在多种细胞通路中调节免疫功能。阻断PCAF和GCN5治疗自身免疫性疾病的机制是通过,减少H3K18、H3K9乙酰化, 抑制NF-κB,IFN-β,TBK1过表达,调节炎症免疫信号。
Compound14:Bassi等人采用PCAF和GCN5的活性抑制剂GSK 4027作为POI配体,采用CRBN作为E3连接酶配体,化合物14能够有效降解PCAF和GCN5,DC50分别为1.5 nM,3 nM。在10 min内,浓度为30 nM的化合物14能使蛋白降解80%。

4 JAK/STAT(Janus激酶信号转导因子/转录激活因子)
JAK/STAT通路是一种重要的细胞内信号传导途径,细胞因子与JAK受体结合,启动STAT转磷酸化,导致增殖和分化等活性的基因表达,引发多种疾病,如类风湿性关节炎(RA)、阿尔茨海默病(AD)、炎症性肠病(IBD)和多发性硬化症(MS)。JAK抑制剂,如Tofacitinib、Ruxolitinib、Baricitinib等,通过调节T细胞活化和自然杀伤(NK)细胞活性,改善类风湿性关节炎。
尽管JAK/STAT靶点已经发现了几十年,但其开发仍存在挑战,如药物半衰期短、血栓栓塞等副作用以及JAK/STAT通路和非典型信号转导之间的串扰。PROTACs可能是破局之选。
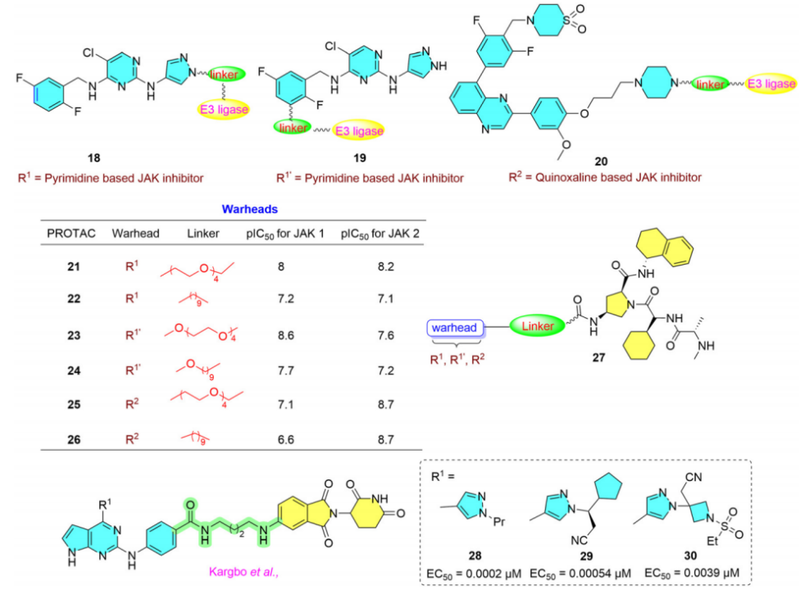
Compound21-26:Shah等人,以嘧啶和喹恶啉核作为POI配体。其中,喹恶啉基序的细胞渗透性优于嘧啶基序,且对JAK2具有更高的选择性,已证明6个PROTACs具有降解JAK1和JAK2的作用。
Compound28-30:Kargbo等人发现化合物28的EC50为0.0002 μM,进一步设计了含有Ruxolitinib、Baricitinib(强效JAK抑制剂)的化学物29和30,EC50分别为0.00054 μM和0.0039 μM。
5 RIPK2(受体相互作用蛋白激酶2)
RIPK2是一种在细胞内信号传导中起关键作用的激酶,参与调节细胞的固有免疫、适应性免疫以及凋亡过程。RIPK2的过度激活和功能失调可导致多种炎症性疾病、自身免疫疾病、癌症以及神经系统疾病。到目前为止,由于泛抑制作用,还没有可用于临床的RIPK2抑制剂。
Compound32-34:Mares等人开发了化合物32,pDC50(DC50的负对数)为9.4± 0.2,但溶解度较差。进一步,通过添加非亲脂性基团来提高溶解度,合成化合物33,pDC50为7.9。进一步,为了解决大剂量依赖性,所合成的化合物34,效力增加了10倍,pIC50为8.0。
Compound35:Bondeson等人开发的化合物35,DC50为1.4 nM,Dmax为95%。

6 STING(人体干扰素基因刺激因子)
Compound45-50:Liu等设计了PROTACs来靶向STING途径治疗各种自身免疫疾病,如系统性红斑狼疮。POI配体为C-170 STING抑制剂,E3连接酶配体为为CRBN,合成连接子长度不同的化合物45-50。其中,化合物47显示出最令人满意的结果,DC50值为3.2 μM。在小鼠肾脏组织中的体内研究表明,化合物47可以以剂量依赖的方式降低IFNβ、IL-6和CXCL-10的水平。

7 MIF(巨噬细胞迁移抑制因子)
虽然MIF以其抗癌潜力而闻名,但它也与免疫反应有关。
Compound51-56:在Xiao等人开发的,以7-羟基香豆素和7-羟基-3,4-二氢苯并恶嗪-2-1核为POI配体,以CRBN为E3连接酶配体的化合物51-56中,化合物54表现最优,在2 μM时,与MIF的Ki值为71%,MIF在A549细胞中降解率为71%。

8 IKZF(Ikaros锌指转录因子)
IKZF对免疫调节活性至关重要,其基因的多态性可导致系统性红斑狼疮。
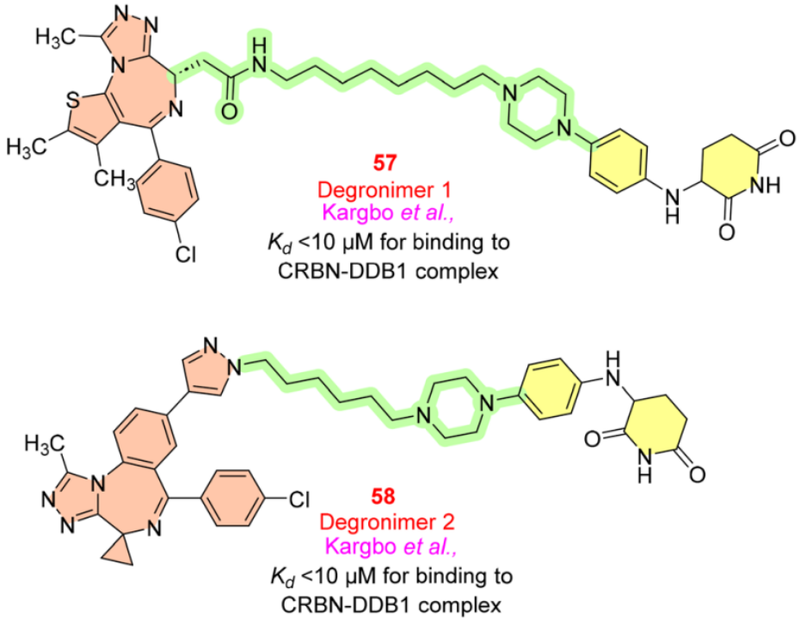
图10 靶向IKZF的PROTACs
小结
PROTACs在探索自身免疫性疾病等靶点方面具有良好的体外效力。在理想情况下,研究人员希望获得高Dmax值(例如大于90%的降解效率)和低DC50值,这意味着PROTAC分子在较低浓度下就能实现高效的蛋白降解,预示着更好的治疗效果和更低的副作用。通过优化PROTAC分子的设计,包括选择合适的靶蛋白(POI)配体、E3连接酶配体和连接子(linker),提高了PROTAC分子的疗效和选择性,有望成功将PROTACs带入自免治疗的临床阶段。
参考资料:
https://doi.org/10.1039/D4MD00142G
公众号内回复“肿瘤免疫”或扫描下方图片中的二维码免费下载《小药说药肿瘤免疫全集》的PDF格式电子书!

公众号已建立“小药说药专业交流群”微信行业交流群以及读者交流群,扫描下方小编二维码加入,入行业群请主动告知姓名、工作单位和职务。
