芪甲柔肝汤(QJ)是一种具有保肝、抗纤维化作用的中药,主要功效在于补益元气、促进血液循环、消除停滞、疏通经络。然而,该药对肠道微生物群落及其代谢产物所产生的影响尚未明确。
近日,一篇名为“Gut microbes combined with metabolomics reveal the protective effects of Qijia Rougan decoction against CCl4-induced hepatic fibrosis”的论文揭示了QJ对CCl4诱导肝纤维化的保护效应。

图1 论文首页
QJ改善CCl4诱导的肝损伤
研究使用40%CCl4诱导HF模型,通过QJ给药6周,并采用血清生化分析、组织病理学、免疫组化、RT-PCR、16S rRNA基因测序和非靶向代谢组学等技术来探究QJ对HF的干预作用。
肝功能检测结果表明,相较于对照组(C组),模型组(M组)的血清天冬氨酸转氨酶(AST)、丙氨酸转氨酶(ALT)以及碱性磷酸酶(ALP)的水平有显著的上升。经QJ处理后,这些指标的水平明显降低(图2B)。此外,QJ处理亦显著降低了HF患者的肝脏指数(图2C)。HE染色结果显示,对照组的肝细胞形态正常,排列紧密,且肝实质内未见明显的病理变化或炎症细胞浸润(图2A)。然而,CCl4处理后,肝细胞出现了明显的脂肪变性、炎症和坏死征兆,而QJ处理能够减轻这些病理变化。
该研究通过qPCR技术检测了各组肝脏炎症指数的变化,结果显示M组的IL-1β、IL-6和TNF-α水平显著升高,而QJ处理显著抑制了这些炎症因子水平的上升,这进一步证实了QJ对CCl4诱导的肝脏炎症具有抑制作用(图2D)。

图2 QJ改善了CCl4诱导的肝损伤
QJ抑制ECM的产生

图3 QJ可减轻CCl4诱导的肝纤维化
QJ改善肠道损伤并上调紧密连接蛋白的表达
C组回肠HE染色切片显示,肠组织结构呈现清晰状态,细胞形态保持正常,未观察到显著的炎症反应(图4A)。CCl4处理组显示出结缔组织排列稀疏,肠绒毛高度及隐窝深度均有所下降,并伴有炎症细胞的浸润。然而,经QJ药物治疗后,肠绒毛高度和隐窝深度得到恢复,且未见明显炎症反应。
紧密连接蛋白作为肠黏膜上皮细胞间的主要连接结构,对于保持肠上皮屏障的结构完整性和功能正常性至关重要。紧密连接的破坏可能导致肠道上皮屏障功能受损,进而使得肠道微生物及其代谢产物的转移,加剧已存在的肝病。研究指出,首次注射CCl4后,小鼠小肠中Occludin的表达显著减少,细菌易位(CCl4,4次)早于肠道微生物失衡(CCl4,24次;桥接纤维化)。肠上皮紧密连接蛋白的改变导致通透性增加,这可能是CCl4诱导肝损伤模型中早期细菌易位的原因。
Claudin-1、Occludin和ZO-1是肠紧密连接蛋白(TJPs)的关键组成部分。研究通过IHC和qPCR测定它们的平均积分光密度(IOD)值和mRNA表达水平。回肠的IHC分析结果(图4A、B)表明CCl4处理后Claudin-1、Occludin和ZO-1的平均IOD值显著下降。尽管如此,经QJ处理后,这些蛋白的表达水平得到恢复。此外,qPCR测量的mRNA表达结果与IHC结果相符(图4C)。结果表明,CCl4模型导致TJPs下调,这可能导致有害肠道微生物及其代谢产物通过肠肝轴影响肝脏,但QJ对CCl4诱导的肠上皮屏障损伤具有积极的修复作用。
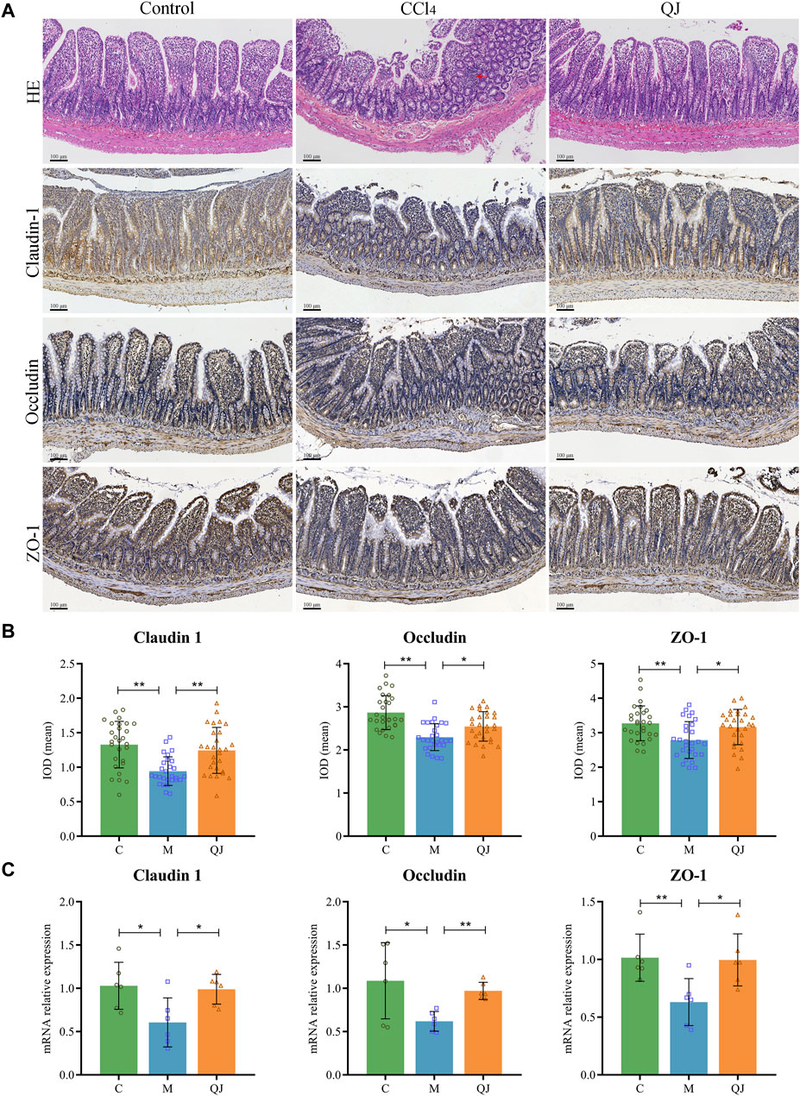
图4 QJ改善肠道损伤并上调紧密连接蛋白的表达
QJ改善CCl4诱导的HF的代谢紊乱
为探究各组的代谢特性,该研究对肠道内容物样本执行了非靶向代谢组学分析。偏最小二乘判别分析(OPLS-DA)揭示了C组与M组、M组与QJ组之间的分离现象。相应的置换检验验证了模型的有效性和可靠性,并未表现出过度拟合现象。火山图揭示了代谢物的差异(图5A、B)。基于M组与QJ组间差异代谢物的分析,研究探讨了QJ抑制HF的代谢途径。相关的KEGG途径包括药物代谢—细胞色素P450、脂肪酸降解、牛磺酸和亚牛磺酸代谢以及赖氨酸降解(图5D)。

图5 QJ改善了CCl4诱导的肝纤维化的代谢紊乱(n=3)
Li X, Xu X, Tao S, Su Y, Wen L, Wang D, Liu J, Feng Q. Gut microbes combined with metabolomics reveal the protective effects of Qijia Rougan decoction against CCl4-induced hepatic fibrosis. Front Pharmacol. 2024 Mar 28;15:1347120. doi: 10.3389/fphar.2024.1347120